
Axetilen C2H2 là một hợp chất hóa học được ứng dụng rất nhiều trong đời sống sinh hoạt cũng như sản xuất công nghiệp. Vậy Axetilen là gì? Hợp chất này có những tính chất nào đặc trưng, được điều chế ra sao, ứng dụng như thế nào và liệu rằng chúng có độc không? Bài viết dưới dây VIETCHEM sẽ cùng bạn đi giải đáp mọi thắc mắc về hợp chất này.
1. Axetilen C2H2 là gì?
Axetilen là một hợp chất hóa học nằm trong dãy đồng đẳng Ankadien với công thức hóa học là C2H2. Nó là một hidrocacbon và là ankin đơn giản nhất.
Trong thực tế, nó không tồn tại ở dạng tinh khiết mà tồn tại ở dạng dung dịch.
Công thức cấu tạo của axetilen: H - C ≡ C - H (viết gọn HC ≡ CH).
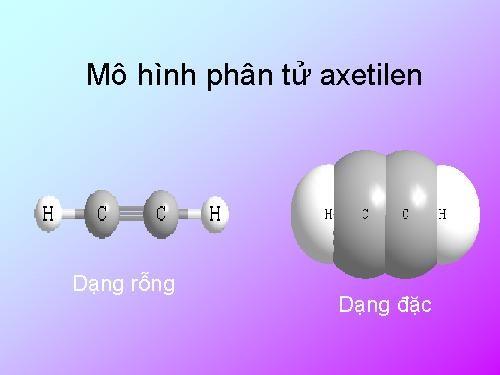
Cấu trúc phân tử của axetilen
Một số tên gọi khác: Acetylene, Ethyne (tên hệ thống IUPAC).
2. Tìm hiểu lịch sử phát hiện axetilen
- Axetilen được phát hiện lần đầu vào năm 1836. Khi Edmund Davy đang thử nghiệm với cacbua kali thì một trong những phản ứng hóa học của ông đã tạo ra một loại khí dễ bắt lửa và đó chính là khí axetilen ngày nay.
- Năm 1859, Marcel Morren đã thành công tạo ra axetilen bằng cách sử dụng các điện cực cacbon để tạo ra một hồ quang điện trong một bầu khí quyển của hidro. Điện hồ quang làm xói mòn các nguyên tử cacbon khỏi các điện cực và liên kết chúng với các nguyên tử hidro, hình thành nên các phân tử axetylen. Ông gọi đó là khí hydro hoá carbon.
- Đến năm 1860, axetilen được tái xuất hiện bởi nhà hóa học người Pháp Marcellin Berthelot. Ông đặt tên cho nó là “acétylène”. Khí axetilen thương mại có thể có mùi hôi do các tạp chất trong nó, phổ biến nhất là hydrogen sulfide và phosphine.
3. Những tính chất đặc trưng của axetilen C2H2
3.1 Tính chất vật lí của Axetilen
- Axetilen là chất khí không màu, không mùi, dễ bắt cháy và tan kém trong nước.
- Tỉ trọng của axetilen với không khí là D= 26/29 và nó nhẹ hơn không khí.
3.2 Tính chất hóa học của Axetilen
- Phản ứng cháy (tác dụng với oxi)
Cũng giống như các hidrocacbon khác như metan, etilen,… axetilen cháy trong oxi tạo ra cacbonic và hơi nước.
2 C2H2 + 5 O2 (t°) → 4 CO2 + 2 H2O
- Phản ứng cộng của axetilen
Axetilen tham gia phản ứng cộng với halogen, hidro halogenua (HCl, HBr,…), AgNO3 trong môi trường amoniac…
Phản ứng cộng với halogen:
HC≡CH + Br-Br → Br-CH=CH-Br
Br-CH=CH-Br + Br-Br → Br2CH-CHBr2
Phản ứng cộng với hidro halogen:
HC≡CH + HBr → CH2=CHBr
Phản ứng cộng với bạc nitrat trong môi trường NH3
HC≡CH + AgNO3 + NH3 + H2O → Ag-C≡C-Ag ↓ màu vàng + NH4NO3
- Phản ứng trùng hợp
Các phân tử C2H2 có thể kết hợp với nhau trong phản ứng trùng hợp và tạo thành polime.
nHC≡CH (t°, xt, p) → (-HC=CH-)n
- Phản ứng hidrat hóa
Axetilen tham gia phản ứng hidrat hóa có xúc tác axit sulfuric để tạo thành sản phẩm cuối cùng là axit axetic theo sơ đồ sau:
HC≡CH + H2O(H2SO4) → H-CH=CH-H → CH3COOH
- Phản ứng cộng
HC≡CH + Br2 → Br-CH=CH—Br (đibrometilen)
HC≡CH + 2 Br2 → Br2CH-CHBr2 (tetrabrometan)
4. Cách điều chế axetilen là gì?
4.1 Điều chế Axetilen trong phòng thí nghiệm
Cho vài mẩu nhỏ canxi cacbua vào ống nghiệm đã đựng sẵn 1ml nước, sau đó đậy nhanh lại bằng nút có ống dẫn khí và đầu vuốt nhọn. Đốt khí sinh ra ở đầu ống vuốt nhọn.
Phương trình phản ứng:
CaC2 + H2O → C2H2 + Ca(OH)2
Phương pháp này sinh ra một lượng nhiệt lớn, hàm lượng canxi cacbua chứa nhiều tạp chất (H2S, NH3, PH3,...) nên axetilen tạo ra không tinh khiết lắm.
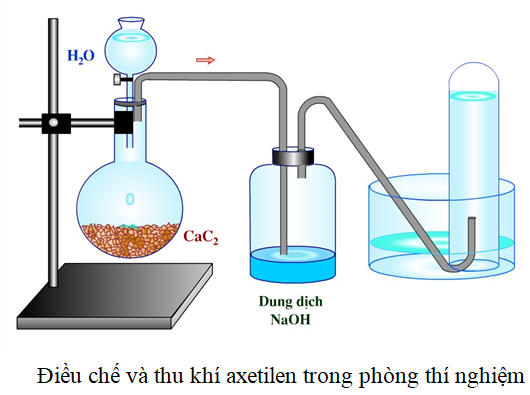
Quy trình điều chế axetilen C2H2 trong phòng thí nghiệm
4.2 Sản xuất Axetilen trong công nghiệp
Phương pháp chủ yếu nhất để điều chế axetilen hiện nay là nhiệt phân metan ở nhiệt độ 15000 °C (phản ứng thu nhiệt mạnh). Vì nhiệt độ sôi của axetilen là -75 °C nên nó có thể dễ dàng được tách ra khỏi hỗn hợp với hidro.
Phương trình nhiệt phân metan (CH4)
2 CH4 → C2H2 + 3 H2
Cho cacbon tác dụng với khí hidro khi có hồ quang điện:
2 C + H2 (hồ quang điện) → C2H2
Điều chế axetilen từ Ag2C:
2 HCl + Ag2C → 2 AgCl + C2H2
Cho canxi cacbua tác dụng với axit sunfuric:
CaC2 + H2SO4 → C2H2 + CaSO4
5. Những ứng dụng của axetilen trong đời sống, sản xuất công nghiệp

Một số ứng dụng của axetilen
>>>XEM THÊM: : Halogen là gì? Những tính chất và ứng dụng quan trọng của halogen
Tuỳ thuộc vào phương thức sử dụng mà chúng ta sử dụng axetilen có độ tinh khiết khác nhau:
- Khí axetilen C2H2 có độ tinh khiết 98% dùng để hàn cắt.
- Khí axetilen 2.5 có độ tinh khiết 99.5%.
- Khí axetilen 2.6, 2.8 có độ tinh khiết 99.6%, 99.8%: Chủ yếu dùng trong phòng thí nghiệm, nghiên cứu, bệnh viện, trung tâm phân tích, viện.
Làm nguyên liệu sản xuất các monome để chế tạo nhiều loại polime khác, ví dụ như sợi tổng hợp, cao su, muội than,…
Dùng làm nhiên liệu trong đèn xì oxi-axetilen (khi được tác dụng với oxy) để hàn, cắt kim loại.
Sản xuất axit axetic, rượu etylic….

Đèn xì oxi - axetilen
6. Axetilen có độc không và những lưu ý khi sử dụng axetilen C2H2 để an toàn ?
- Nếu tiếp xúc với khí axetilen dưới 2,5% trong khoảng thời gian dưới 1 giờ thì con người sẽ an toàn.
- Nếu nồng độ axetilen vượt quá mức phép: Nạn nhân sẽ cảm thấy buồn nôn, đau tức ngực, khó thở, nhức đầu, đi loạng choạng, da tái xanh, đau phổi, hôn mê. Tiếp xúc với da sẽ gây nên tình trạng phát ban.
- Vì axetilen là chất dễ nỗ và dễ bắt cháy nên cần được bảo quản nơi khô ráo, thoáng mát, tránh nguồn phát nhiệt và các loại hóa chất khác. Ngoài ra, nơi cất giữ cần có rào che chắn cẩn thận, có bảng hiệu cẩn thận.
7. Một số bài tập áp dụng về Axetilen
Bài tập 1: Cần bao nhiêu ml dung dịch brom 0,1M để tác dụng hết với:
a) 0,224 lít etilen (ở đktc).
b) 0,224 lít axetilen (ở đktc).
Lời giải
a) Phương trình hóa học:
CH2=CH2 + Br2 → CH2Br-CH2Br
Ta có: nBr2 = nC2H4 = 0,224/22,4 = 0,01 (mol)
⇒ Thể tích của dung dịch Brom là:
V dd Br2 = 0,01/0,1 = 0,1 (lít) = 100 ml
b) Phương trình hóa học
HC≡CH + 2Br2 → Br2-CH-CH-Br2
Ta có: nBr2 = 2nC2H4 = 2 x (0,224/22,4) = 0,02 (mol)
⇒ Thể tích của dung dịch Brom là:
V dd Br2 = 0,02/0,1 = 0,2 (lít) = 200 ml
Bài tập 2: Biết rằng 0,1 lít khí etilen (đktc) có thể làm mất màu tối đa 50 ml dung dịch brom. Vậy nếu dùng 0,1 lít khí axetilen (ở đktc) thì có thể làm mất màu tối đa bao nhiêu ml dung dịch brom trên?
Lời giải:
Phương trình hóa học
CH2=CH2 + Br2 → CH2Br-CH2Br
HC≡CH + 2Br2 → Br2-CH-CH-Br2
Từ phương trình hóa học, chúng ta có thể thấy lượng axetilen có thể làm mất màu dung dịch brom nhiều gấp đôi etilen => 0,1 lít khí C2H2 có thể làm mất màu tối đa 100 ml dung dịch Br2.
Bài tập 3: Tiến hành đốt cháy hoàn toàn 11,2 lít hỗn hợp khí gồm C2H2 và C2H4 thu được 12,6 gam nước và khí CO2. Hãy tính phần trăm thể tích của mỗi loại khí trong hỗn hợp trên (đktc).
Lời giải:
Gọi số mol của C2H4 và C2H2 lần lượt là x và y mol.
nkhí = v/22,4 = 11,2/22,4 = 0,5 (mol)
→ x + y = 0,5 (1)
PTHH:
C2H4 + 3O2 → 2CO2 + H2O
x 2x mol
2C2H5 + 5O2 → 4CO2 + 2H2O
y y mol
nnước = m/M = 12,6/18 = 0,7 mol
Theo các PTHH có: nnước = 2x + y = 0,7 (2)
Từ (1) và (2) có x = 0,2 mol và y = 0,3 mol
Do các khí ở cùng điều kiện nên tỉ lệ về thể tích cũng chính là tỉ lệ về số mol
→ %V (C2H4) = nC2H4 / nhh . 100% = 0,2/ 0,5 . 100% = 40%
% V (C2H2) = 100% -40% = 60%
8. Mua axetilen ở đâu uy tín, chất lượng tại Hà Nội, tp. Hồ Chí Minh?
Trên thị trường hiện nay, hóa chất axetilen C2H2 được bán khá phổ biến. Tuy nhiên, không phải nơi nào cũng bán axetilen đảm bảo chất lượng, giá thành. Vậy mua axetilen ở đâu đảm bảo chất lượng, giá cả. Đây không phải là câu hỏi khó, cũng không phải câu hỏi dễ vì nếu bạn biết đến công ty Vietchem thì đây là một câu hỏi không hề khó. Bởi lẽ, Vietchem chính là địa chỉ cung cấp axetilen cho thị trường toàn quốc, được đông đảo khách hàng, từ các tập đoàn, doanh nghiệp lớn đến các cá nhân nhỏ lẻ.
Khi đến với Vietchem, các bạn không chỉ nhận được sản phẩm tốt, giá thành cạnh tranh mà các dịch vụ từ tư vấn đến giao nhận hàng cũng rất chuyên nghiệp.
Vậy nếu bạn nào đang băn khoăn chưa biết mua hóa chất axetilen ở đâu thì hãy liên hệ ngay với chúng tôi theo số HOTLINE 0826 010 010 để được các bạn tư vấn viên báo giá và hỗ trợ TỐT nhất.
Link nội dung: https://topnow.edu.vn/axetilen-h2-a67349